红星资本局9月23日消息 9月22日晚,亚宝药业(600351.SH)公告称,公司对SY-009研发项目进行了审慎评估,决定终止SY-009的临床研究开发工作。
红星资本局注意到,SY-009为亚宝药业的糖尿病新药项目,早在2018年7月就获批进入临床试验,目前仍停留在Ⅱ期临床研究阶段,该公司为其研发投入共计8786.98万元。
近年来,全球口服降糖药市场竞争激烈。除了国内药企旗下达格列净二甲双胍缓释片陆续获批,GLP-1受体激动剂(GLP-1RA)类别的新型降糖药物研发进展也备受关注。
亚宝药业终止糖尿病新药研发
后续研发投入巨大且存不确定性
据亚宝药业公告,SY-009是一种钠-葡萄糖协同转运蛋白 1(Sodium-glucose Cotransporter1SGLT1)抑制剂,可以降低餐后葡萄糖的吸收,公司拟开发成用于2型糖尿病患者治疗的口服制剂。
从研发情况看,2018年7月,SY-009获得国家药监局核准签发的《药物临床试验批件》,2019年4月至2024年3月期间完成3项Ⅰ期临床研究和1项Ⅱ期临床研究。2024年9月,SY-009获得国家药监局核准签发的新增适应症《药物临床试验批件》,批准了SY-009针对功能性便秘开展Ⅱ期临床试验的申请。
一款早在七年前就拿到临床试验批件的糖尿病新药,为何选择终止?亚宝药业解释称,根据SY-009的Ⅱ期临床研究结果,主要疗效终点未达到,如果补充增加Ⅱ期临床剂量探索试验再开展Ⅲ期临床试验所需时间较长,后续研发投入巨大且存在较大不确定性;同时SY-009针对功能性便秘的Ⅱ期临床研究尚未开展,后续研发也存在较大不确定性。

截图自亚宝药业公告
据亚宝药业2024年年报,SY-009项目属于该公司多个创新药项目之一,原计划完成时间为2031年5月。结合该公司最新公告来看,SY-009研发投入共计8786.98万元,其中费用化金额3207.65万元,资本化金额5579.33万元。
亚宝药业称,根据相关会计政策,基于SY-009项目已终止临床研究开发且相关专有技术尚未找到潜在可出售对象的实际情况,出于谨慎性考虑,公司对SY-009项目研发资本化金额5579.33万元全额计提资产减值准备,这将减少公司2025年度利润总额5579.33万元。
资料显示,亚宝药业成立于1978年,2002年在上交所上市,主要产品有中西药制剂、贴敷剂、原料药和药用包装材料等300多个品种,涉及儿科领域、成人药以及大健康产品。该公司最为外界所知的产品是儿科品种丁桂儿脐贴,是治疗儿童腹泻用药的独家专利产品。
IQVIA 2024年数据显示,丁桂儿脐贴在地级市市场份额达19%,同比提升3个百分点,持续领跑儿童止泻外用品类市场。2024年,亚宝药业实现营业收入26.86亿元,同比减少7.69%;实现归母净利润2.43亿元,同比增长21.60%。亚宝药业称,营收下降主要系盐酸倍他司汀注射液、丁桂儿脐贴等主要产品收入减少。
全国糖尿病市场规模超700亿
国产口服降糖药陆续获批
红星资本局梳理发现,SY-009并非亚宝药业针对2型糖尿病适应症的首个研发项目。2024年下半年,该公司结合目前糖尿病新型药物的研发上市情况和同靶点药物的研究进展,对SY-008项目的研究结果进行综合评估后,认为继续开发的风险较高,终止了后续临床研究。
公开资料显示,SY-008由亚宝药业旗下苏州亚宝与礼来共同研发,同样是用于治疗2型糖尿病的化药1类口服制剂,早在2016年12月临床试验获批,后完成了Ia和Ib期临床研究。截至2024年末,该公司已就SY-008累计投入研发费用2950.65万元。
红星资本局注意到,全球口服降糖药市场竞争激烈,SGLT2抑制剂、二肽基肽酶4(DPP-4)抑制剂、二甲双胍类是主要畅销类别。根据摩熵医药数据库统计显示,2023年全国医院口服降糖药销售额TOP10中,阿斯利康旗下的达格列净片(SGLT-2抑制剂)位列第一,其中医院端40.89亿元,药店端19.53亿元。
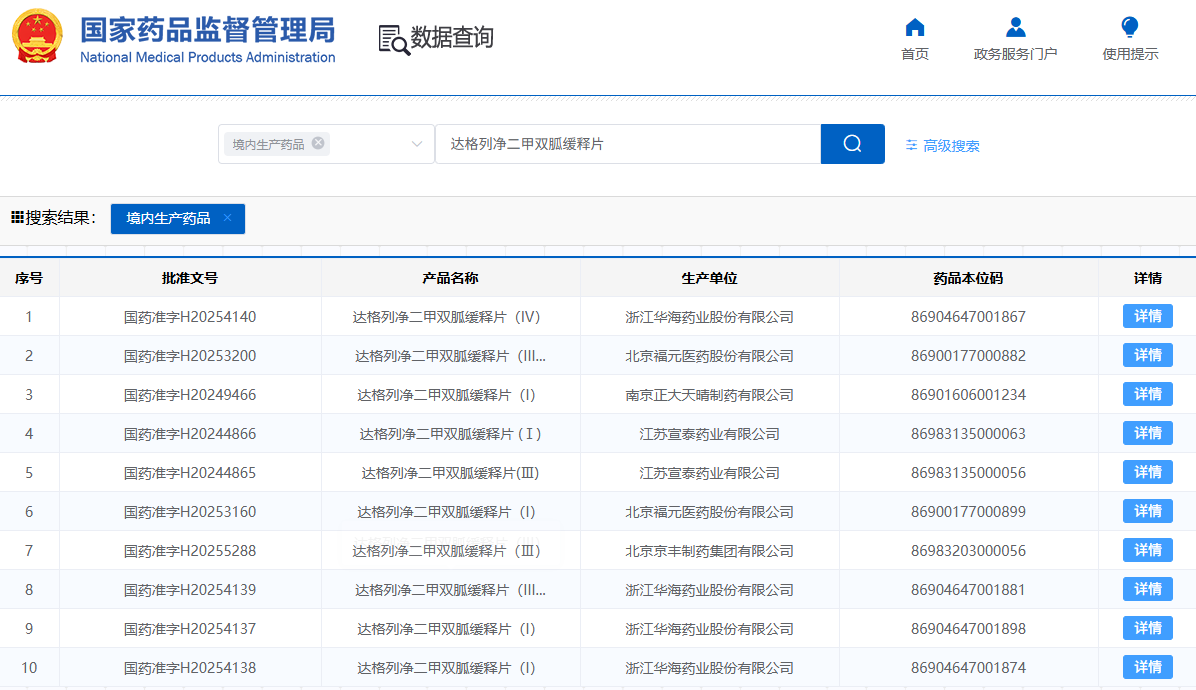
国内厂商则将目光瞄准达格列净二甲双胍缓释片。据国家药监局官网,截至目前,国内已有华海药业(600521.SH)、福元医药(601089.SH)、南京正大天晴、江苏宣泰药业等7家药企获得该药品生产批文。
此外,近年备受关注的新型降糖药物GLP-1受体激动剂(GLP-1RA)也迎来口服版。今年1月,诺和诺德旗下降糖版司美格鲁肽口服制剂在中国获批上市,为全球唯一获批的口服GLP-1药物,仅获批用于治疗成人2型糖尿病。8月,信达生物(1801.HK)宣布口服小分子GLP-1R激动剂IBI3032的新药临床试验申请(IND)获美国FDA批准。
国元证券研报近期指出,2024年全球糖尿病市场规模接近800亿美元,我国糖尿病市场规模也超过700亿元。GLP-1RAs凭借更好的降糖效果,更低的副作用销售额快速增长,逐步取代其他传统降糖药的市场份额,预计趋势有望继续。随着对GLP-1药物研发的逐步深入,口服药成为了GLP-1未来发展的核心趋势之一。

