资本眼
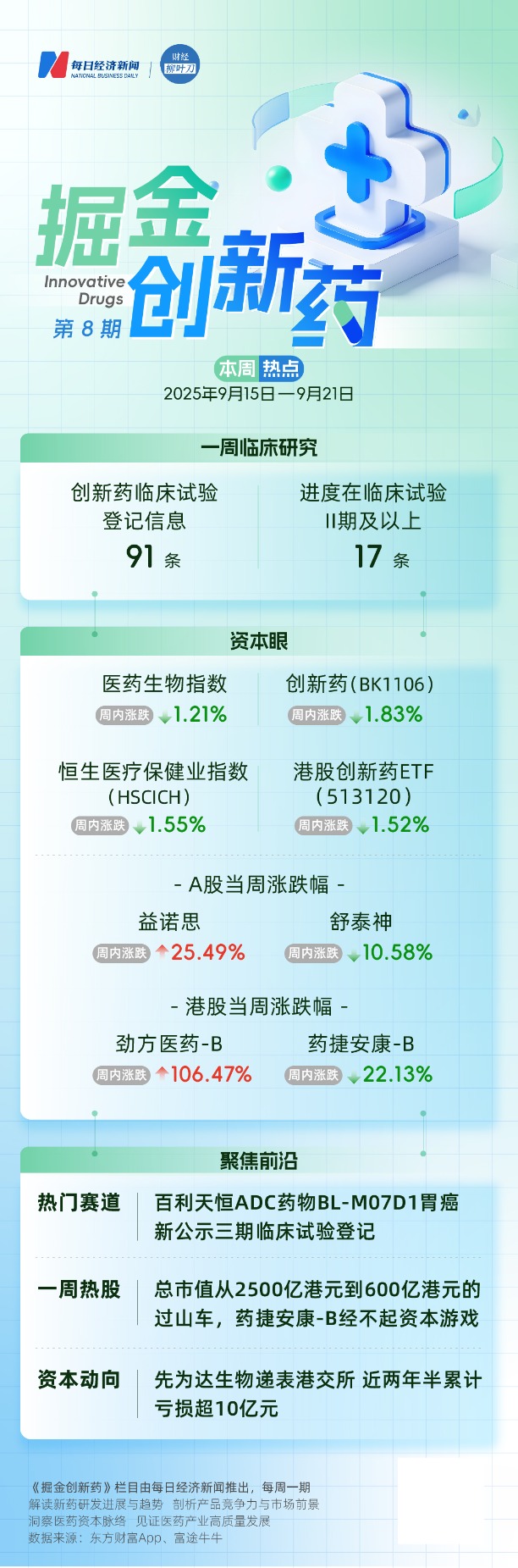
一周行情
9月15日至9月19日,医药生物指数下跌1.21%,跑输上证指数0.91个百分点。创新药(BK1106)周内下跌1.83%。恒生医疗保健业指数(HSCICH)周下跌1.55%,港股创新药ETF(513120)周内下跌1.52%。
一周IPO动向
先为达生物递表港交所,近两年半时间累计亏损超10亿元
9月19日,港交所官网披露,杭州先为达生物科技股份有限公司(以下简称“先为达生物”)提交A1上市申请书。
先为达生物成立于2017年,以GLP-1等大分子药物研发为核心,身处当下最热门的减重赛道。2024年底,公司核心产品埃诺格鲁肽注射液(XW003)向国家药品监督管理局提交超重/肥胖症及2型糖尿病两项适应证的上市申请,预计在2026年初获批上市。
今年6月21日,一项关于埃诺格鲁肽(Ecnoglutide,曾用名伊诺格鲁肽)的Ⅲ期临床试验(SLIMMER研究)结果发表在《柳叶刀·糖尿病与内分泌学》杂志上。
SLIMMER研究是目前中国最大样本量的减重药物Ⅲ期临床试验,在全国36个中心入组664例肥胖(BMI≥28kg/m²)或超重(BMI≥24kg/m²)且伴有至少一种体重相关合并症的患者,随机接受每周一次埃诺格鲁肽1.2mg、1.8mg、2.4mg或安慰剂治疗48周。
结果显示,每周注射该药物的受试者在48周治疗期间体重最多可减轻13.8公斤,而注射安慰剂的受试者仅减重约200克。
此外,接受埃诺格鲁肽治疗的受试者在停药后仍能维持减重效果,在7周内体重仅反弹约1%。
目前,XW003已实现BD(商务拓展)授权。2024年,先为达生物与韩国Hk Inno.N合作,授权XW003在韩国地区权益。2025年1月,其与英国Verdiva Bio达成协议,授予其口服XW003等产品在除大中华区及韩国以外的全球独家开发与商业化权利,首付款近7000万美元、潜在交易总额超24亿美元。
招股书显示,先为达生物在2023年、2024年均无收入,其他收入及收益分别为6403万元、3435万元;研发开支分别为4.56亿元、2.84亿元;期内亏损分别为6.2亿元、4.86亿元。
2025年上半年,先为达生物营收为9107万元,毛利为8001万元,其他收入及收益为1602万元,期内亏损为1.08亿元。
截至2025年6月30日,先为达生物持有的现金及现金等价物为7.8亿元。
创新眼
一周临床试验动向
根据医药魔方提供的数据,9月8日至9月12日,国家药品监督管理局药品审评中心共披露91条临床试验登记信息。其中,17条处于临床试验II期及以上的临床试验登记信息,主要针对肿瘤领域。
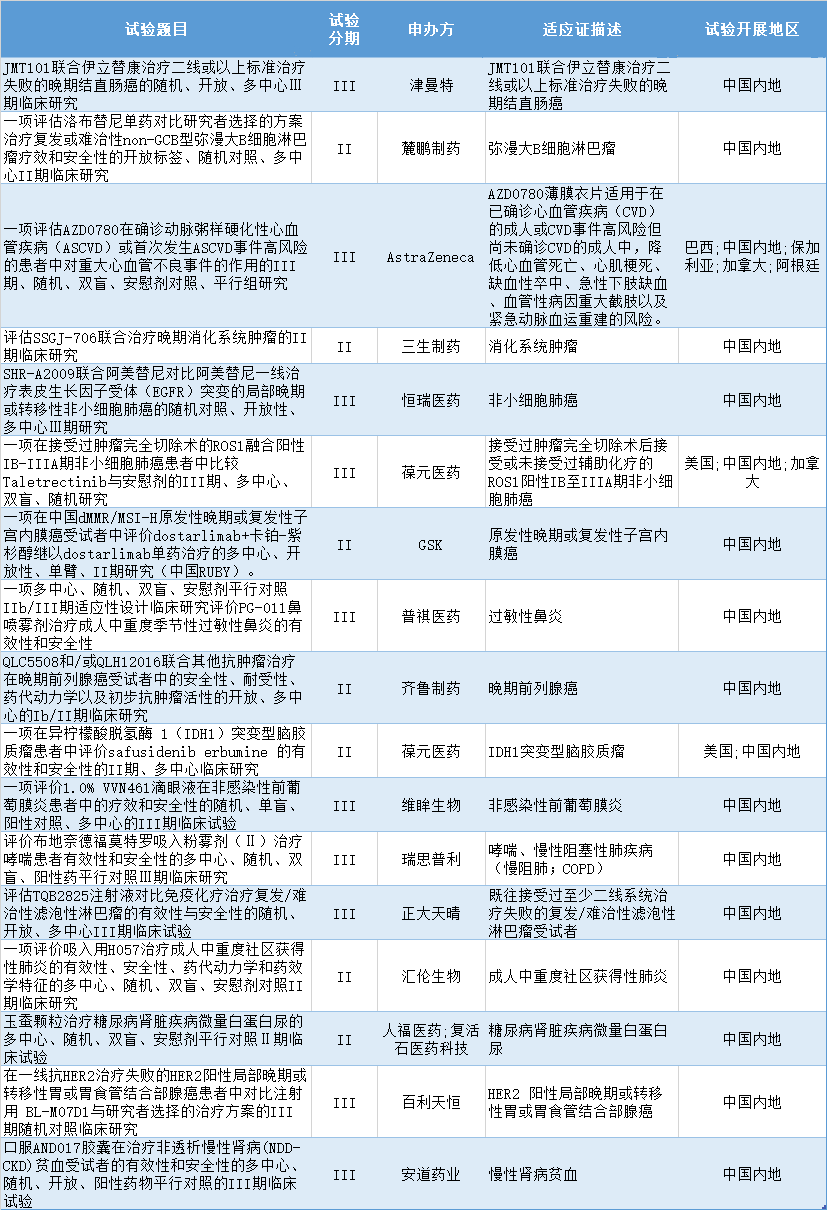
数据来源:医药魔方
前沿洞察
一周热股
药捷安康-B:股价过山车,创新药经不起资本游戏
过去三个月,药捷安康-B曾怒涨超50倍,市值一度接近2700亿港元大关,创下港股“资本奇迹”,9月16日,药捷安康突然上演高台跳水,股价从679.5港元/股掉落至192港元/股,堪比“过山车”,资本游戏戛然而止。
对于一家成立仅11年、尚未有任何产品商业化、上半年仍亏损1.23亿元的生物医药公司而言,亏损似乎并不是太大的问题,管线预期才是硬道理。药捷安康的看点便是核心产品替恩戈替尼(Tinengotinib,TT-00420)。
从竞争格局看,替恩戈替尼是唯一同时覆盖FGFR/VEGFR、JAK和Aurora靶点组合的药物,在耐药实体瘤领域占据先发优势。但其最具竞争力的胆管癌、前列腺癌适应证对应的市场空间有限。因此,在医药行业人士看来,这一产品支撑不了千亿港元市值。
对于这一轮震荡,市场普遍认为是由于该公司被纳入港股通创新药指数后,带来了ETF的被动买入效应,多个ETF因此成为了“接盘侠”。市场对国证港股通创新ETF的质疑声日益高涨,认为其纳入这样的新兴公司成分股的决策缺乏合理性。此外,药捷安康的股价波动也显露出港股市场的高风险特征,尤其是对尚未实现商业化的企业。
百利天恒ADC BL-M07D1胃癌新公示三期临床试验登记
医药魔方数据显示,9月15日,百利天恒新登记一项临床试验:一线抗HER2治疗失败的HER2阳性局部晚期或转移性胃/胃食管结合部腺癌患者中对比注射用BL-M07D1与研究者选择的治疗方案的III期随机对照临床研究。
BL-M07D1是具有抗肿瘤活性的靶向HER2的抗体偶联药物(ADC),采用的是拓扑异构酶抑制剂类小分子毒素Ed-04以及Ac接头,药物具有更佳的亲水性,同时不易聚集,在体内具有更高的安全性和抗肿瘤活性。临床前研究表明,在不同肿瘤模型中,BL-M07D1均优于第一三共的同靶点HER2-ADC药物DS-8201。
今年6月23日,BL-M07D1用于在新辅助治疗后存在浸润癌残留的HER2阳性乳腺癌术后辅助治疗的III期临床试验完成首例受试者入组,目前正在国内外开展12项临床试验,包括肺癌和消化道肿瘤等。
本次更新的临床登记显示,该研究为二线治疗方案,71个研究中心目标入组490人、入组年龄为18岁到75岁,尚未招募患者。主要研究机构为哈尔滨医科大学附属肿瘤医院、复旦大学附属肿瘤医院;主要研究者为张艳桥、郭伟剑。
该研究的主要重点为总生存期(OS)和无进展生存期(PFS);次要终点有5个:治疗期间出现的不良事件,治疗相关不良事件;总缓解率/客观缓解率,持续缓解时间,疾病控制率;免疫原性;无进展生存期;PK/PD特征。
云顶新耀耐赋康被纳入全球肾脏病权威指南
9月19日,云顶新耀宣布,其核心产品耐赋康(布地奈德肠溶胶囊)被纳入全球肾脏病权威指南《2025KDIGO IgA肾病和IgA血管炎临床管理实践指南》,成为该指南中唯一被推荐的IgA肾病对因治疗药物。
据了解,IgA肾病是一种以免疫球蛋白A(IgA)免疫复合物沉积在肾小球中为特征的肾脏疾病,该疾病会导致肾脏发炎和损伤,并可能进展为慢性肾功能衰竭。我国IgA肾病患者基数庞大,据统计,国内约有500万IgA肾病患者,每年新增确诊病例超12万人。
破局者故事
腾讯健康总裁吴文达:AI制药是临床前研究变革性的工具,腾讯的定位很清晰,就是用模型驱动提高研发效率
一款创新药物的研发过程大致可分为三个阶段,靶点假说的提出与药物靶点确定、潜力分子优化与临床前候选化合物评估,以及最后的临床试验验证。过去,药物研发通常需要十几年的时间、10亿美元至15亿美元的投入,成功率却只有十分之一。
AI(人工智能)则有可能改变这一切。“木头姐”凯茜·伍德曾在今年年初强调,从长远来看,医疗保健可能会成为最深刻的AI应用领域。
具体到医药研发上,有人把AI制药定义为第三代药物革命。目前,国内的AI制药聚焦于临床前研究,作用主要体现在三个方面:一是加速靶点发现和化合物设计;二是降低实验失败率;三是优化资源分配。虽然临床前研究成本占比不高,但AI在这一阶段的效率提升有助于后续的临床研究,最终可以降低整体研发成本和时间。
腾讯在AI制药领域布局已久,十年前投资“AI制药第一股”晶泰控股,在国内较早做蛋白质结构预测,2020年推出AI驱动药物研发平台“云深智药”。现在,腾讯AI制药平台成果进展如何?相比同赛道玩家,其竞争优势是否得以体现?目前的AI制药技术对药物研发带来了哪些改变,还面临怎样的挑战?在“2025腾讯全球数字生态大会”召开期间,腾讯健康总裁吴文达接受了《每日经济新闻》记者的采访。

