2025年9月7日是第十二个世界杜氏肌营养不良症(DMD)知晓日。这种让男童逐渐失去行走能力、累及心肺的遗传病,正困扰着中国约7万名患者——平均来说,中国每5000名新生男婴中,就有1名患病。
目前,皮质类固醇药物是DMD的标准治疗方案,可以将患者的中位生存期延长超过10年,但国内专家提供的数据显示,近半数中国患者从未用过激素药物,国内激素治疗规范率仅23%。
不过,随着国内首款DMD创新激素药物——伐莫洛龙(Vamorolone)于去年获批,患者依赖地夫可特(Deflazacort)“临时进口”救命的历史告一段落。随着伐莫洛龙口服混悬液(商品名:安迦利)通过基本目录形式审查,该药物有望参与今年的国家医保谈判。
中国约有7万名患者,接受标准治疗寿命可延长超过10年
与大部分罕见病一样,杜氏肌营养不良症是一种由基因突变引起的遗传性疾病。具体来说,其病因是DMD基因突变导致抗肌萎缩蛋白缺失,引发进行性肌肉萎缩和无力,常伴心脏与呼吸系统并发症。
杜氏肌营养不良症是一种X连锁遗传病,即由X染色体上的异常基因引起。男性只有一个X染色体,无法像女性携带者可能还有一个正常X染色体进行补偿,所以男性的患病率大幅高于女性。
目前,全球约有25万名DMD患者,每5000名新生男婴中就有一人患病;中国是世界上DMD患者人数最多的国家之一,预估约有7万名DMD患者。
值得注意的是,根据《中国杜氏肌营养不良携带者筛查的临床实践指南》,约30%的DMD患儿为基因突变,其余约70%的患儿的母亲是携带者,因此DMD携带者筛查是降低患儿出生率的关键。
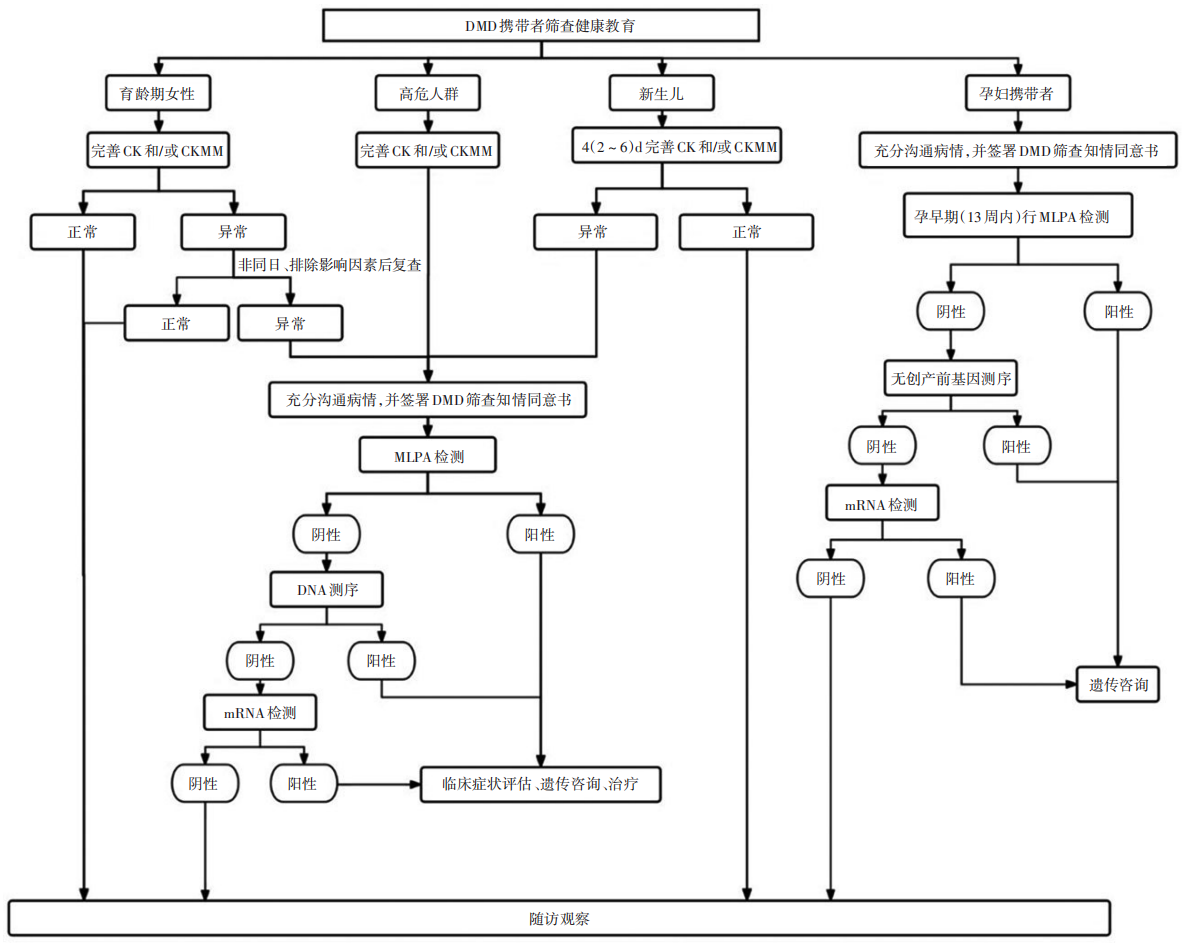
DMD携带者筛查流程图图片来源:《中国杜氏肌营养不良携带者筛查的临床实践指南》
对于已经确诊DMD的患者,多学科综合管理可延缓病情并提高生活质量。资料显示,依据病情进展,DMD可分为五期,在中国,DMD患者的死亡中位年龄约为18.57岁,当前标准治疗下患者中位生存期达28.7岁,较未接受治疗延长超过10年。中国区域研究显示,规范治疗者生存期为24.8~27.9岁。
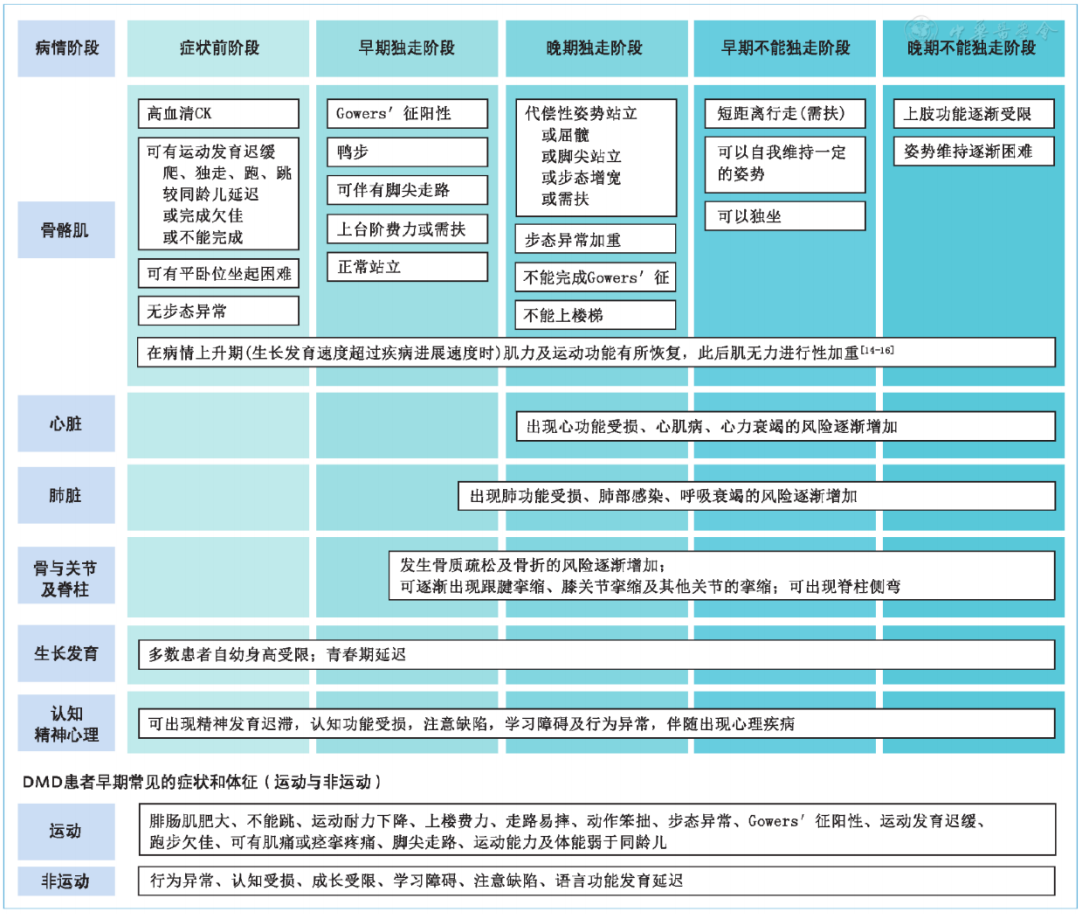
DMD患者的主要临床表现及其病情演变图片来源:《Duchenne型肌营养不良多学科管理专家共识》
近半数患者从未用过激素药物,国内首款新药于去年获批
皮质类固醇药物目前是DMD的标准治疗方案。北京协和医院神经科副主任、主任医师戴毅教授建议,患者在3岁以后就应该进行积极的激素治疗,但目前国内的激素治疗规范率仅23%。
北京大学第一医院罕见病医学中心袁云教授提供的数据显示,2015年,中国DMD患者的激素治疗率只有26.3%,2020年提升至54%,但目前仍有近半数患者从未用药。
除了筛查、诊断水平仍待提升,激素治疗的缺失也与药物缺乏有关。
一方面,传统激素的长期使用,会导致生长发育落后、骨质疏松、肥胖、多毛、易怒等副作用,严重影响患儿的身心健康。
另一方面,全球首款用于治疗杜氏肌营养不良症的糖皮质激素——地夫可特至今未在国内正式获批,为了满足国内患者的用药需求,自去年2月起,该药物只能通过“临时进口”途径进入中国,并在北京协和医院等医疗机构定点使用。
不过,去年12月,CDE(国家药品监督管理局药品审评中心)批准了国内首款专门用于治疗杜氏肌营养不良症的药物——伐莫洛龙。资料显示,伐莫洛龙是一种糖皮质激素类药物,同时也具有对盐皮质激素受体的拮抗作用,具备双重作用机制,其原研厂商为瑞士Santhera制药公司。
2023年10月和2023年12月,该药物先后在美国、欧盟获批,在美国获批的适应证是用于治疗2岁及以上的杜氏肌营养不良症患者,在欧盟获批的适用患者年龄则是4岁及以上。2022年1月,曙方医药从Santhera制药公司引进该药物,该药物在中国的获批适应证为治疗4岁及以上的杜氏肌营养不良症患者。
今年8月,伐莫洛龙口服混悬液通过了基本目录形式审查,有望参与今年的国家医保谈判。
全球仅一款基因治疗药物获批,已有国产同类药物获批临床
近年来,CGT(细胞与基因治疗)作为生物医药领域的重要方向,也逐渐成为DMD新药研发的热点。
戴毅教授告诉《每日经济新闻》记者,在DMD领域,广义的基因治疗包括外显子跳跃药物,目前全球已有多款药物获批上市,这类药物主要在基因转录过程中发挥调节作用,并不会改变患者的基因组;而狭义的基因治疗,则特指基因替代或基因编辑疗法,目前全球仅一款相关药物获批上市,即Sarepta和罗氏共同开发的Elevidys。
2023年6月,美国FDA(美国食品药品监督管理局)通过加速审批途径,批准Elevidys用于4~5岁可行走的DMD患者;2024年6月,该药物的适用人群年龄扩展至4岁以上,覆盖约80%的DMD患者。
由于定价高达320万美元/针(约合人民币2300万元/针),Elevidys曾刷新全球最贵药物纪录,目前仍是史上第二贵的基因治疗产品。不过,该药物此前因涉及患者死亡事件,陷入了不小的争议。
戴毅教授表示,无论是狭义还是广义的基因治疗,其与激素药物的核心区别在于更侧重于疾病上游的病因,即在基因缺陷层面进行修正。从原理上看,基因治疗药物似乎更具备“治本”潜力,但全球获批的多款外显子跳跃药物,临床效果并不理想,不能简单理解成“基因治疗药物一定优于激素药物”。
记者注意到,今年4月,信念医药的BBM-D101注射液获批国内临床试验申请(IND),目前处于临床研究阶段。该药物与Elevidys都属于重组腺相关病毒(rAAV)基因治疗药物,其目标是通过单次静脉输注实现“一次给药、长期有效”的治疗效果。9月5日,由戴毅教授主持的该药物注册类临床研究(CTR20252461)已完成首例受试者给药。

