央广网北京4月1日消息(记者齐智颖)科创板拟上市公司苏州同心医疗科技股份有限公司(下简称“同心医疗”)更新招股书及财务数据。根据招股书,2025年该公司实现营业收入近2.13亿元,同比增长175%,同时相较于2023年收入增长超3倍。
从收入结构看,同心医疗产品在国内外市场均实现快速增长。国内方面,该公司已获批上市CH-VAD产品及配件的销售收入从2023年5006.16万元增长至2025年1.05亿元,同比增长100%;海外方面,该公司BrioVAD产品及配件从2024年首次实现收入1026.35万元,到2025年收入增至1.07亿元,增长超10倍,占公司整体收入50.51%。同时,BrioVAD 系统毛利率达72.28%。
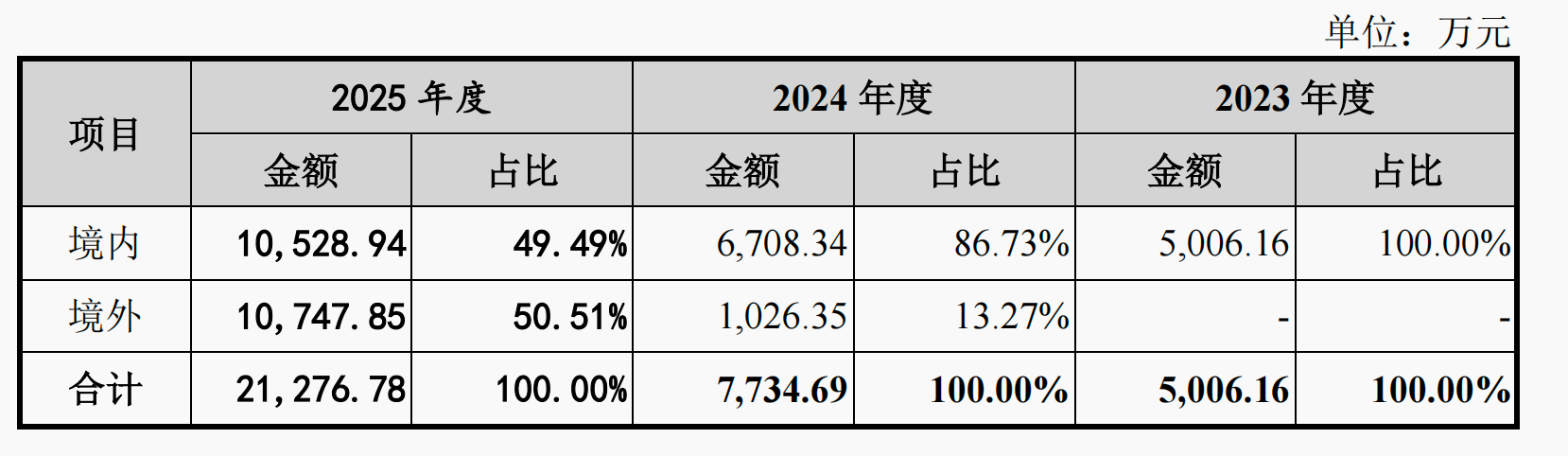
图片来源:同心医疗最新招股书
招股书显示,经过十多年源自底层的全面科技创新和技术积淀,同心医疗已形成针对超小型全磁悬浮式人工心脏的多学科多目标优化、磁悬浮轴承原理与构造、流体力学优化、能源与信息传输等一系列关键技术。公司据此自主研发的 CH-VAD、BrioVAD 等产品是被监管和国际学界广泛承认的全磁悬浮式人工心脏,在血液相容性、防感染性、植入侵犯性等评价植入式人工心脏的各项关键性能方面,均展现出具有全球竞争力的技术优势和潜在临床价值。得益于长期技术积淀,公司持续创新,正在开展新一代植入式人工心脏 BrioVAD 2.0 的研发,取得了多项技术性突破。
从招股书公开数据来看,截至本招股书签署之日,同心医疗在国内累计完成超过750例CH-VAD的植入。其迭代版本CH-VAD Plus目前也已经获得国家药监局批准上市。
同心医疗BrioVAD已获得FDA的IDE批准开始临床试验,未来拟通过PMA这一美国最严格的医疗器械审查流程申报上市,BrioVAD 获批进入美国临床试验标志着公司在高风险、高复杂性医疗器械的设计控制、风险管理、过程验证等方面达到国际前沿水平,是我国自主开发的高风险医疗器械进入美国市场的重要里程碑。同心医疗表示,该临床试验随后获得美国医保体系覆盖,平均每例支付约22万美元,使公司在临床试验阶段即实现收入。
公开资料显示,同心医疗BrioVAD美国临床试验自2024年获批以来,持续提速。2024年11月完成首例患者植入;2025年8月,BrioVAD美国临床试验获得FDA批准进入确证性阶段。截至更新版招股书签署之日,BrioVAD美国临床试验已在美国26家中心累计完成152例患者植入(含对照组)。该临床试验计划将覆盖全美植入量领先的60家顶尖医学中心。
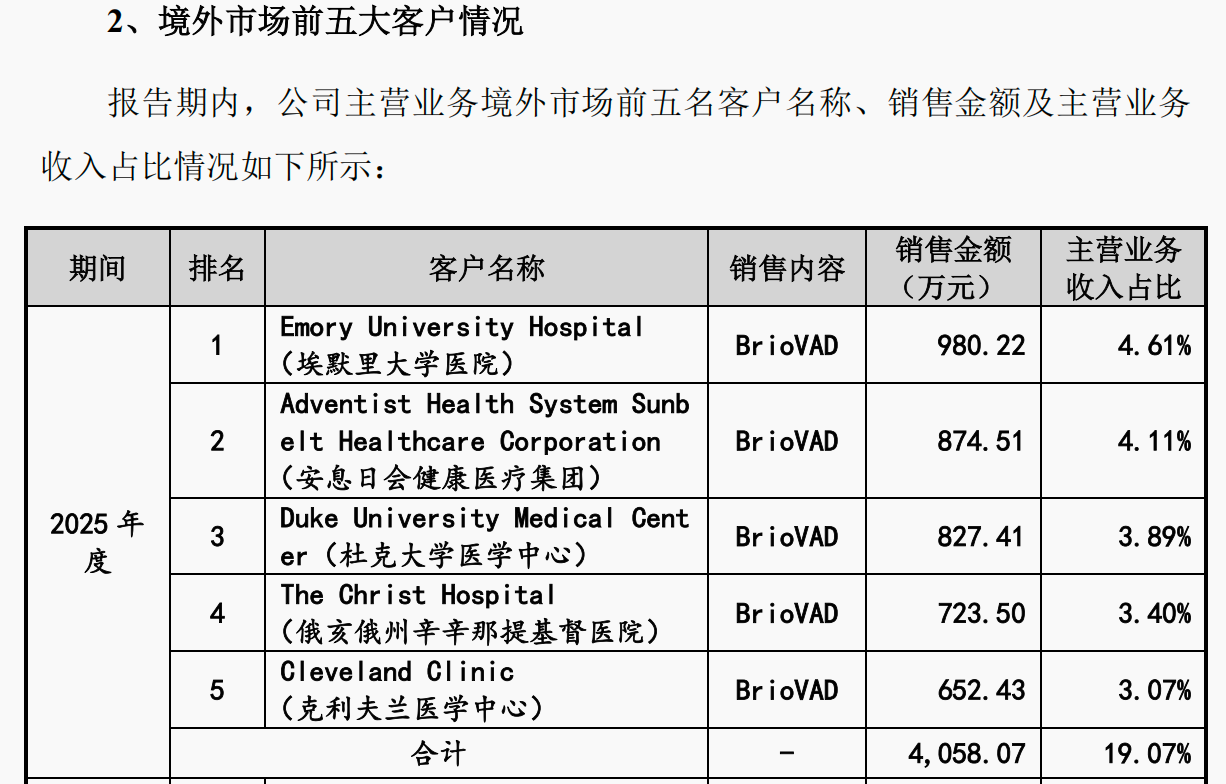
图片来源:同心医疗最新招股书
在欧洲市场,同心医疗在德国、奥地利和荷兰递交了临床试验申请并已获得德国伦理委员会的批准。截至更新版招股说明书签署日,公司已与2家中心完成临床试验协议的签署。此外,公司正在推动BrioVAD适应症向儿童晚期心衰扩展,拟开展Brio4Kids在美国、日本的联合研究,同心医疗称,已于2026年3月正式向FDA递交临床试验申请。

