如果一个医学发现不仅能拿下“诺奖风向标”的大奖,还能吸引全球超50款药物前仆后继地研发,它该有多大的魅力?如果身经百战的跨国药企都折戟于此,它又该有多高的壁垒?
这不是一个假设,而是整合素αvβ3靶点过去40年面临的真实处境。如今,破局者终于出现,而且来自中国。
近日,国家药品监督管理局(NMPA)通过优先审评审批程序,批准佛山瑞迪奥医药有限公司(北京吉伦泰医药有限公司控股子公司)申报的1类放射性创新药锝99mTc佩昔瑞特加肽注射液(99mTc-3PRGD2)上市,主要用于可疑肺癌患者区域淋巴结转移的辅助检查。
该产品是一款放射性核素偶联药物(RDC),是我国首个自主研发的1类创新核药,也是全球首个用于SPECT显像的广谱肿瘤显像剂。
最为重要的是,这款产品是全球首个以整合素αvβ3为靶点成功上市的1类创新核药药物。这一进展,标志着一个被研究近40年的“明星靶点”,正式跨越基础研究与临床应用之间的关键鸿沟。
整合素:“诺奖潜力”靶点的临床转化之痛
想要了解该款产品的意义,得先了解整合素αvβ3曾经带给全球医药行业的痛苦。
整合素是一类细胞表面跨膜受体,由α和β两种亚基非共价结合形成异二聚体,介导细胞与细胞外基质的黏附,并参与信号传导及微环境调控。目前已知整合素由18种α亚基和8种β亚基组合成24种不同的受体类型,在免疫反应、凝血、伤口愈合及肿瘤转移中均发挥关键作用。
在整个整合素家族中,αvβ3因其在肿瘤生物学中的特殊角色而成为“明星靶点”。该受体在正常成年人体内表达极低且分布局限,但在胶质母细胞瘤、乳腺癌、前列腺癌、黑色素瘤等多种肿瘤细胞表面呈现高表达,并通过介导内皮细胞黏附和迁移,在肿瘤血管生成、肿瘤细胞增殖、侵袭及转移中起关键调控作用。
整合素的发现始于上世纪80年代。理查德·O·海因斯(Richard O. Hynes)、埃尔基·罗斯拉赫蒂(Erkki Ruoslahti)与蒂莫西·A·斯普林格(Timothy A. Springer)三位科学家因在该领域的奠基性贡献,于2022年被授予素有“诺奖风向标”之称的拉斯克医学奖(Lasker Award)[1],也使整合素相关研究被广泛认为具备冲击诺贝尔奖的科学价值。
尽管整合素αvβ3的科学价值毋庸置疑,但从1986年该靶点首次被鉴定以来,全球制药界对这一靶点的探索屡屡受挫。据2023年《Pharmacological Research》综述统计,全球至少有15款靶向整合素αvβ3的药物进入临床试验阶段,若是算上所有衍生物和不同适应症的探索,这一数字超过50款[2]。
比较有代表性的受挫案例是默克公司开发的西仑吉肽(Cilengitide)。作为一种αvβ3/αvβ5双重抑制剂,它曾是首个进入Ⅲ期临床的整合酶抑制剂,被寄予治疗胶质母细胞瘤的厚望。然而,2013年其Ⅲ期CENTRIC研究未能达到主要终点,相关开发最终被终止。类似的项目还有阿斯利康旗下MedImmune公司的Etaracizumab(伊瑞西珠单抗)和强生公司的Intetumumab(英妥木单抗),均因疗效不足而未能进入临床Ⅲ期[3]。
这些失败基本上都源于药代动力学特性不佳、靶点抑制不完全、易产生信号通路代偿等问题,也揭示出整合素靶向药物的深层困境:传统的“阻断”策略或许无法应对整合素信号调控的复杂性,这在相当长的时间内动摇了行业对整合素靶向策略的信心。
研发破局:中国学者“巧妙超车”
当跨国巨头还在“死胡同”不断碰壁时,中国学者选择另辟蹊径。如今,中国首个1类创新核药锝99mTc佩昔瑞特加肽注射液(99mTc-3PRGD2)正式获批,不仅打破了近40年的研发僵局,也引爆了全球医药界对整合素αvβ3的全新想象。
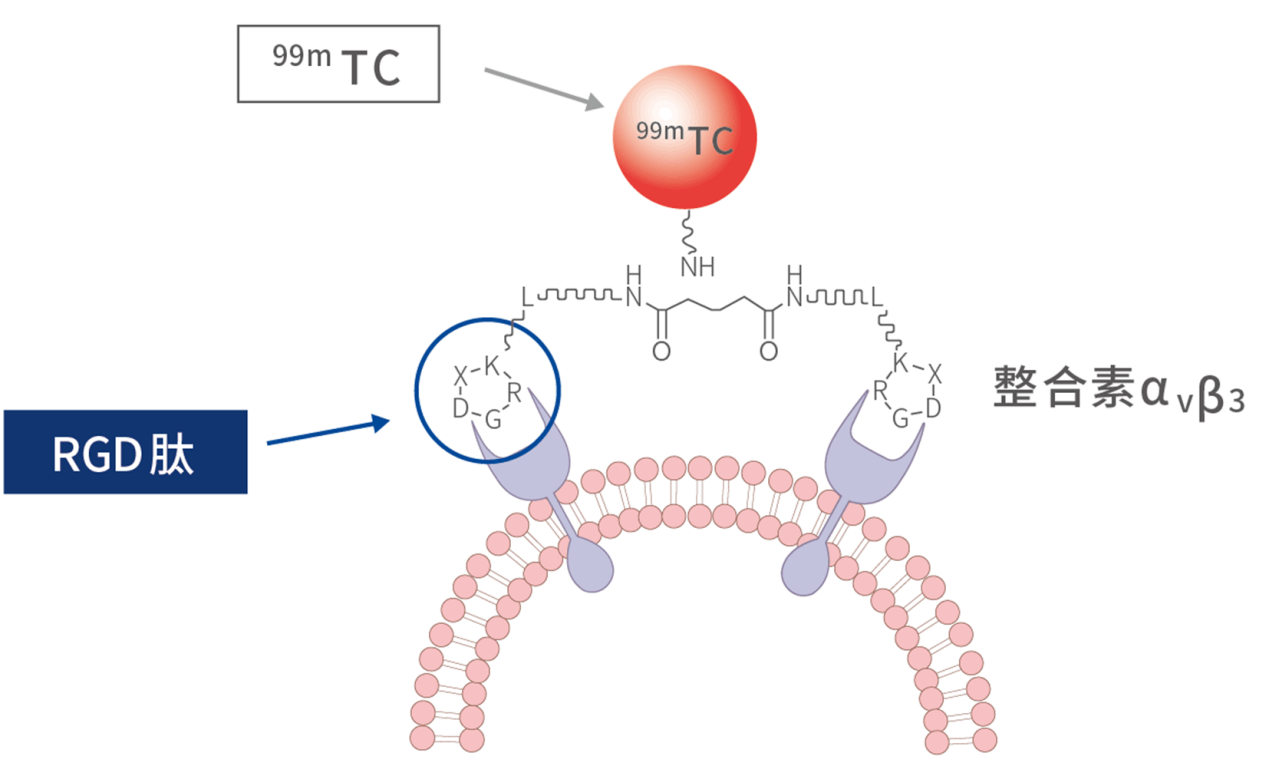
99mTc-3PRGD2是一款核素偶联药物(RDC),即通过连接子(Linker)将靶向载体的探针(RGD多肽)和放射性核素结合,探针负责识别和结合αvβ3靶点,核素作为放射源实现显像。这一设计使药物的作用逻辑发生了根本性转变——它不试图抑制整合素功能,也不杀伤整合素高表达的细胞,而是利用整合素αvβ3作为“锚点”,将放射性核素精准递送至肿瘤部位进行显像。
这一策略的实现,建立在扎实的分子设计基础之上。吉伦泰公司创始人王凡教授及其团队提出“间隔基团修饰”理论,在两个RGD模序之间引入PEG4柔性连接剂,设计了新型RGD多肽二聚体。该二聚体通过两个RGD序列的协同作用,使与整合素αvβ3的结合亲和力达到纳摩尔(nM)级别,远优于传统单体RGD肽,实现对受体高选择性、强亲和力的特异性识别[4]。
得益于高亲和力特性,该探针在临床显像中仅需较低给药剂量即可实现有效靶向富集。同时,分子设计上仅作为靶向示踪载体,虽可高效结合受体,却不诱导整合素发生功能性构象变化,也不产生明显的信号激活或拮抗效应,因此不会干扰整合素介导的正常生理调控过程[5]。正是这一“利用靶点而非攻击靶点”的技术路线,为整合素αvβ3长达近40年的转化困境提供了全新的解法。
如此精妙的设计,到底能给患者带来什么实实在在的好处?
临床数据表明,此次被国家药监局批准上市的99mTc-3PRGD2SPECT不仅在肺部肿瘤良恶性鉴别诊断上与金标准18F-FDG PET/CT无统计学差异,其特异性和准确性显著高于18F-FDG PET/CT,纠正了59%18F-FDG PET/CT显像淋巴结转移假阳性结果,显著降低淋巴结转移灶的误诊率,极大地提高临床诊断的精准度,尤其是肿瘤分期、随访的可靠性[6]。同时,凭借更简便的药物制备流程、更高普及率的SPECT设备及更低的患者检查成本,大幅提升了核医学诊疗的临床可及性。基于αvβ3在多种肿瘤细胞高表达的特性,99mTc-3PRGD2SPECT未来也有望在乳腺癌、胶质瘤等领域拓展诊断市场[7]。
产业资本护航,破浪核药“诊疗一体化”蓝海
作为全球首个获批的整合素αvβ3靶向药物,99mTc-3PRGD2的价值远不止于诊断领域。其先发优势更在于为后续治疗药物的开发铺设了“验证轨道”——这正是核药“诊疗一体化”特性的核心所在。
核药具备独特的“诊疗一体化”优势:同一靶向载体搭配不同核素,可实现“诊断核素定位、治疗核素杀伤”的闭环。诊断核素用于精准定位肿瘤,治疗核素则利用同一靶向分子实现精准治疗。99mTc-3PRGD2作为全球首个获批的整合素αvβ3靶向药物,其临床成功验证了该靶点的成药可行性,为后续靶向αvβ3的治疗性核药或偶联药物开发提供了关键的临床验证基础。
正是看中了核药“诊疗一体化”的潜力,国内深谙产业孵化的百洋医药集团早早便作为“伯乐”入局。2022年,百洋医药集团战略投资吉伦泰公司,旗下上市公司百洋医药(SZ.301015)获得了包括99mTc-3PRGD2、99mTc-HP-Ark2等多款吉伦泰公司自主研发的放射性药品商业化权益。
医药源头创新是一个漫长且复杂的工程,研发周期长、环节多、壁垒高,单家企业难以独立完成全链条布局。科学家创业更是面临“九死一生”的挑战,生产要素配套不足、专业团队缺失,成为成果转化的关键瓶颈。医药创新从研发立项、临床前研究到临床试验、注册审批等,每个环节都需专业团队支撑,任一环节疏漏都可能导致项目失败。
作为专注于医药健康领域的产业投资人,百洋医药集团凭借完善的产业生态和专业的创新孵化能力,补齐科学家创业短板,通过产业资源配置和全方位赋能支持深度参与,推动创新成果从实验室走向临床,真正落地成药。
从产业视角看,百洋的“提前下注”逻辑也非常清晰:一方面,通过成熟的商业化能力,将锝99mTc佩昔瑞特加肽注射液(99mTc-3PRGD2)这一更有临床优势和更具可及性的核药产品快速导入临床,惠及更广泛的患者群体;另一方面,看中的是αvβ3这一靶点背后的诊疗一体化平台价值——诊断产品的成功,有望撬动更大的治疗市场。随着靶点临床价值的加速验证,围绕αvβ3的治疗性药物开发路径将大幅缩短,而百洋通过提前锁定该靶点的核心资产,已然占据这一赛道的先发位置。
结语
2022年拉斯克医学奖授予整合素发现者时,学界再次热议诺奖的可能性。然而从靶点发现到临床应用,整合素αvβ3走了整整40年。99mTc-3PRGD2的获批,补上了整合素αvβ3靶点“从实验室到临床”的最后一环,基础科学发现最终转化为惠及患者的药物,中国医药创新将在这一重磅靶点的临床转化史上留下浓墨重彩的一笔。
从更宏观的角度来看,吉伦泰创始人王凡教授及其团队的成功是中国医药创新从“跟随式创新”向攻坚“全球首创”蜕变的绝佳注脚,更提供了一个“科学家源头创新与成熟产业生态的深度融合”的样本:通过百洋医药等产业力量的全方位赋能,科学家得以跨越成果转化的“死亡之谷”,让实验室的成果真正转化为挽救生命的武器。
伴随资本赋能与研发的持续深入,αvβ3的进一步研究、更多适应症的拓展,以及诊疗一体化模式的长期验证,均有望取得新的突破。在核药这片星辰大海中,一个由中国引领的核医学时代,或许刚刚启幕。

