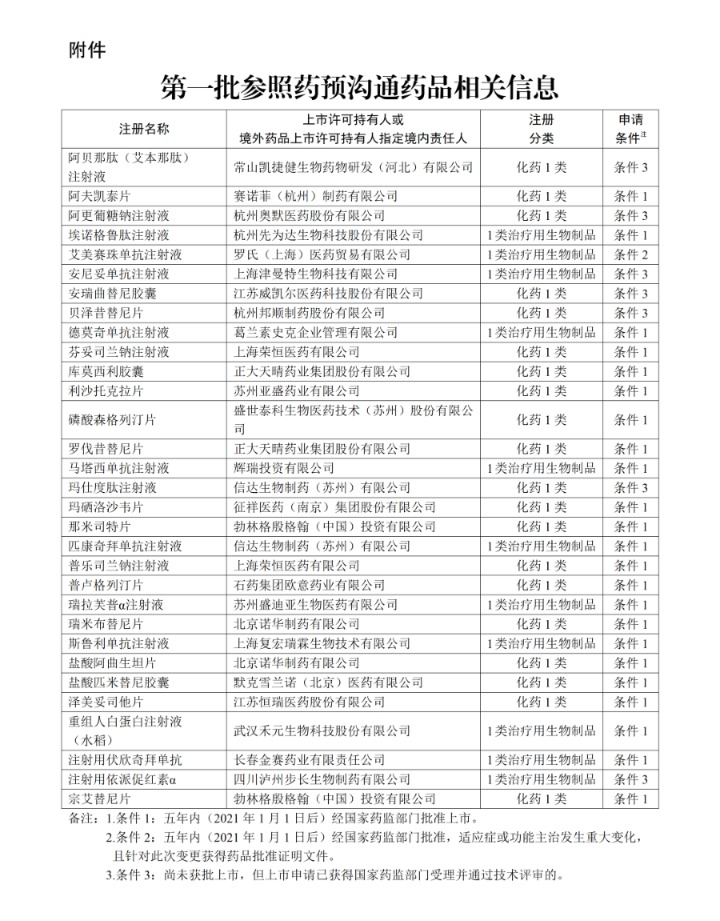
近日,国家医保局公示第一批参照药预沟通药品信息,共31个1类创新药,涵盖肿瘤、代谢、自身免疫等领域,涉及恒瑞、信达、亚盛、罗氏、诺华等中外头部药企。
从上市情况看,23个为五年内新上市药品,1个为五年内适应症或功能主治发生重大变化的药品,另外7个则为尚未获批上市药品。
在业内看来,这是为新一轮医保目录调整做铺垫。我国医保谈判已长期采用参照药比价机制,既往流程为企业先建议参照药,医保评审专家在此基础上遴选确定最终参照药,二者可能会存在差异,且最终参照药在谈判前才明确,易导致企业报价策略缺乏稳定预期。
为此,国家医保局单独设立参照药预沟通环节,并将其列入2026年医保“高效办成一件事”首批重点工作,明确2026年至少开展2轮预沟通。2月10日,国家医保局发布《参照药预沟通办法(试行)》,从制度层面规范并保障该项工作落地。
而此次参照药预沟通的核心意义在于,在正式谈判启动前,由企业自愿申请、医保局组织专家论证并出具参照药建议,可明确谈判比价基准;企业据此能针对性开展卫生技术评估与定价策略准备。未来,参照药预沟通将成为行业提前研判年度医保谈判竞争格局的重要窗口。
涵盖31个药品
当前药品市场环境变化较快、竞争激烈,上市后尽快选择合适的参照药对药品特别是创新药找准市场定位、比较临床价值有重要意义。
目前,我国在医保药品目录调整时引入了选择参照药的做法,这是国际医保准入的通行做法,是测算药品医保支付标准的重要锚点。企业在申报时,可以建议参照药,评审专家据此结合临床实际确定参照药,为后续专家测算提供参考。
国家医保局此前发文指出,因药物经济学等的研究需要时间,一般企业会按自己建议的参照药先行开展药物经济学评价,如果评审确定的参照药与企业的不同,可能会导致整个药物经济学报告没有可参考性,测算专家不得不采用其他路径来进行评估。
2025年6月30日,国家医保局会同国家卫健委出台《支持创新药高质量发展的若干措施》,明确提出加强创新药在药品目录准入方面的政策指导,进一步加强政企沟通交流。
在此基础上,国家医保局明确,参照药预沟通工作先从五年内获批上市,以及适应症或功能主治发生重大变化的1类新药起步。考虑到审批时间因素,尚未获批上市但国家药监部门已受理上市申请,且已通过技术评审的1类新药也可提前申请。
首批参照药预沟通药品纳入31个药品,其中20个为化药1类,11个为1类治疗用生物制品。多个药品在2025年已冲刺基本医保目录。盛世泰科生物于2024年12月获批的磷酸森格列汀片,石药集团欧意药业于2025年1月获批的普卢格列汀片,二者均为DPP-4抑制剂,用于改善成人2型糖尿病患者的血糖控制。
在企业提供的参照药品名单中,磷酸森格列汀片与普卢格列汀片分别选择了苯甲酸福格列汀片、苯甲酸阿格列汀片,前者为2024年6月在我国获批的1类创新药;后者为2013年在我国获批进口上市的产品,日均费用分别为4.05元、8.07元。
可见,受临床定位与比价策略等多重因素影响,即便作用机制一致,企业在自行选择参照药时,也可能在考虑各种因素后有不同的倾向。而这,也不一定最终与评审专家确定的参照药一致。
另有几款产品在2025年尝试进入首版商保创新药目录,但最终并未成功,包括罗氏的艾美赛珠单抗注射液、复宏汉霖的斯鲁利单抗注射液,以及金赛药业的注射用伏欣奇拜单抗,且金赛药业的产品属于医保、商保双轨布局。
其中,艾美赛珠单抗注射液于2018年11月在我国获批上市,适用于部分成人及儿童血友病患者的常规预防治疗,当前国内无同适应症、同机制、同治疗模式的药物;注射用伏欣奇拜单抗于2025年6月在我国获批上市,是中国首款且唯一获批急性痛风性关节炎适应症的1类创新生物制剂,二者均属于“First-in-Class”(首创新药)药物。
企业在申报这两款药品时,建议参照药品一栏均为空白,有业内人士认为,这客观上导致企业缺少明确的药品参照锚点,会为其药物经济学评价建模、医保谈判或商保协商的价值测算带来现实难点。而参照药预沟通,将有效破解这些难题。
药价形成机制加速变革
梳理名单可以发现,部分企业的两款药品进入首批参照药预沟通药品公示名单,比如勃林格殷格翰的那米司特片和宗艾替尼片,信达生物的玛仕度肽注射液和匹康奇拜单抗注射液,正大天晴的库莫西利胶囊和罗伐昔替尼片。
亚盛医药的利沙托克拉片也在首批参照药预沟通药品公示名单中。作为中国首个上市的国产原创Bcl-2抑制剂,利沙托克拉片可谓打破了进口垄断,同时也是全球第二个上市的Bcl-2抑制剂。利沙托克拉片作为1类新药,符合参照药预沟通政策条件,也为药品进入国家医保药品目录、真实世界研究奠定了基础。
此外,常山凯捷健生物的阿贝那肽(艾本那肽)注射液、上海津曼特生物的安尼妥单抗注射液等7款尚未上市的产品也被纳入该公示名单。2026年新一轮国家医保谈判格局正逐步清晰。
需要说明的是,国家医保局此前明确,医保部门在药品目录调整、医保综合价值评估、真实世界研究等工作中将优先考虑论证推荐的参照药和主规格,但由于是提前沟通,可能会出现市场环境、循证证据等变化,如因特殊情况不采用的,应当提出明确的理由或依据。对于没有参加预沟通的,如果企业申请纳入医保目录,专家评审阶段仍会讨论确定参照药和主规格。
这是我国药品价格形成机制改革的一大缩影。医保支付标准对药品价格的形成具有重要的引导作用,随着参照药预沟通工作的持续推进,药企在开展医保谈判前可以有更准确的价格预期,有效提升谈判筹备效率与决策确定性。
与此同时,国务院办公厅近日发布的《关于健全药品价格形成机制的若干意见》(简称《意见》),从顶层设计方面持续优化医保谈判环节药价形成机制。
《意见》明确,要兼顾患者获益和鼓励创新,优化医保目录调整规则。对申报纳入医保目录的独家药品,在医保基金可承受的前提下,综合首发价格合理性等因素,与医药企业谈判形成与经济社会发展水平和市场规模相匹配、合理体现药品临床价值的支付标准。
不仅如此,《意见》从全周期、全渠道、全领域的角度提出了一系列改革举措,健全以市场为主导的药品价格形成机制,推动医药产业高质量发展。
有业内人士认为,参照药预沟通机制可被视为《意见》落地的重要一步,可以让医保谈判更加公开透明,也能有效缓解药企定价与医保准入之间的信息不对称,减少非理性报价与反复博弈。在保障医保基金可持续运行、减轻患者用药负担的同时,也给创新药企发展吃了一颗“定心丸”。