近年来,我国儿童心脏移植事业步入加速提质的高质量发展阶段,但供心短缺依旧是制约重症心衰患儿临床救治的核心瓶颈。国家儿童医学中心、上海交通大学医学院附属上海儿童医学中心心脏中心团队最新研究表明,通过拓宽供心选择范围、普及心室辅助装置应用、攻坚异种移植技术三大核心路径,能够显著提升儿童终末期心脏病救治水平,为更多濒临绝境的心衰患儿带来重生希望。
我国儿童心脏移植事业始于1995年,由中山大学附属第一医院完成国内首例儿童心脏移植手术,正式开启这一领域的临床探索。相关数据显示,全国儿童心脏移植手术量已从2015年的14例稳步增长至2024年的148例,年均增幅显著。但严峻的现实是,我国每年约有4万名心衰患儿住院治疗,其中相当一部分患儿病情会持续进展为终末期心脏病,当前的移植手术规模,远远无法满足庞大的临床救治需求。
科学合理扩大供体适配范围,多举措扩大供心来源
儿童供心短缺是全球器官移植领域共同面对的难题。业内专家提出,适度放宽供受者体重匹配比例、规范开展ABO血型不相容心脏移植、标准化运用心死亡器官捐献(DCD)供心,能有效扩充可用供心储备。
目前国内外临床实践均已证实,科学合理扩大供体适配范围,不会明显增加手术安全风险,还能大幅缩短患儿等待供心的时间。以上海儿童医学中心为代表的国内顶尖儿童心脏诊疗机构,已成功完成婴幼儿ABO血型不相容心脏移植手术,为低龄、危重患儿打通了全新的生命救治通道。
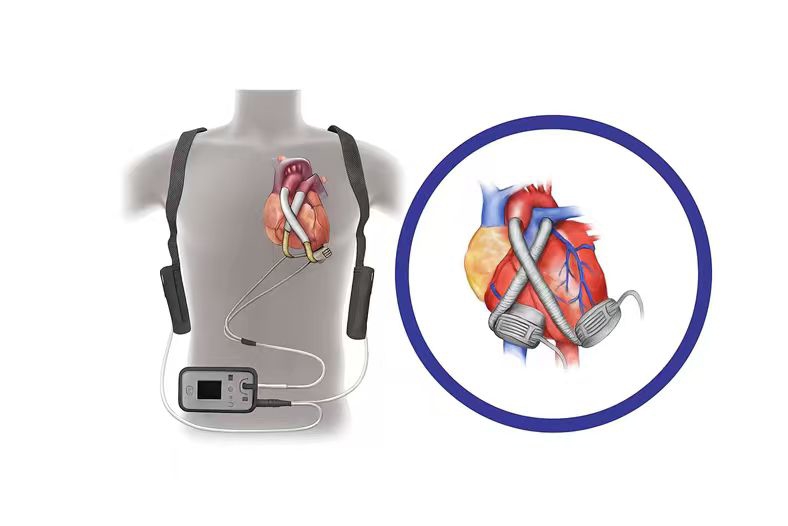
心室辅助装置搭建“生命桥”,为移植与康复争取时间
当合适供心无法及时匹配到位时,心室辅助装置(VAD)成为衔接患儿生命的关键支撑。第三代磁悬浮离心泵凭借运转效率高、术后并发症少等突出优势,既能维持患儿正常血液循环、为等待心脏移植争取宝贵时间,部分患儿甚至可借助该装置实现心脏功能康复,最终成功撤机。
国际临床数据显示,经心室辅助装置支持6个月后,超八成患儿能获得理想的预后效果。随着国产心室辅助设备陆续获批上市,我国儿童机械循环支持技术水平实现快速提升。但现阶段国内仍缺乏适配婴幼儿的专用心室辅助装置,微型化、微创化的婴幼儿专属器械,已成为未来研发的重点方向。
异种移植实现技术突破,未来有望从根源破解供心困境
基因编辑猪-人异种心脏移植已在国际上取得重要临床突破,而儿童免疫系统尚未发育成熟,具备更好的免疫耐受性,让儿科异种移植拥有天然优势。
未来,经过精准基因编辑的异种心脏,可作为“生物人工心脏”,为危重婴幼儿提供短期生命支持过渡,最终顺利完成同种异体心脏移植。若能成功攻克免疫排斥、伦理规范、法律法规等关键难题,异种移植技术将有望从根本上解决长期困扰儿童心脏移植的供心短缺困局。
依托专科诊疗优势,提升复杂先心病移植救治精准度
复杂先天性心脏病患者,尤其是单心室Fontan术后出现心脏衰竭的患儿,已逐渐成为儿童心脏移植的主要受众群体。这类病例心脏解剖结构复杂、机体免疫敏感度高、合并病症多样,移植手术难度极大。
专家强调,充分依托儿童专科医院在先天性心脏病诊疗上的专科优势,通过精准的供受体匹配、个性化手术方案设计、精细化围手术期全流程管理,能够有效提升复杂病例的心脏移植成功率。
据悉,该核心研究内容已整理成学术论文《中国儿童心脏移植的机遇与挑战》,近期发表于《中华器官移植杂志》,由上海儿童医学中心张浩、郑景浩、祝忠群、傅立军团队共同完成。心血管学科带头人张浩教授表示,我国儿童心脏移植已从早期探索阶段,正式迈入高质量发展新阶段。

